-
پنجشنبه, ۲۹ آبان ۱۳۹۹، ۰۷:۵۴ ب.ظ
-
۱۵۴۱

تماس بگیرید:
09129227565

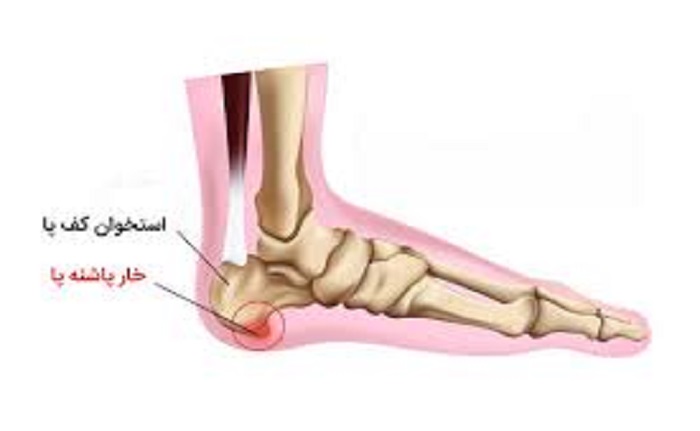
| پارکینسون این بیماری همان لرزش در وضعیت استراحت است که شیوع آن بیشتر در سنین پیری است اما در جوانان هم دیده میشود شیوع آن در تمام مناطق دنیا یکسان است یعنی درصد شیوع بیماری با تغییر در منطقه خیلی فرق نمیکند. بهطور کلی این بیماری بر اثر از بین رفتن سلولهای ترشحکننده مادهای به نام دوپامین (که یک انتقال دهنده عصبی) است رخ میدهد. افزایش نسبتاستیل کولین به دوپامین در غدههای قاعدهای مغز موجب علائم ترمور، سفتی عضلات و کندی حرکات میشود. |
علائم پارکینسون
پارکینسون بر اساس دو علامت یا بیشتر از چهار علامت اصلی بیماری مشخص میشود. ارتعاش و لرزش دست و پا در حالت استراحت، کندی حرکات، سختی و خشک شدن دست و پا و بدن و نداشتن تعادل این چهار علامت اصلی را تشکیل میدهند.
در مراحل اولیه بیماری، ارتعاش اندام ملایم و معمولاً در یک طرف بدن وجود دارد و احتیاجی نیز به درمان ندارد اما با پیشرفت بیماری فردی که دست لرزان خود را در جیب یا پشت خود پنهان میکند یا چیزی را برای کنترل ارتعاش مدام در دست میگیرد، دیگر قادر به پنهان کردن لرزشهای شدید اندام به ویژه به هنگامی که میخواهد تمرکز بیشتری به خود دهد نیست.
چهار علامت شایع بیماری ارتعاش دست و پا در حالت استراحت (لرزش بیمار همزمان با ارتعاش دست و پا در حالت استراحت) آرام شدن حرکت (برادیکینزیا / Bradykinesia) سختی حرکت (و خشک شدن) دست و پا یا بدن تعادل بد (تعادل ضعیف) در حالی که دو یا بیشتر از این علایم در بیمار دیده شود، مخصوصاً وقتی که در یک سمت بیشتر از سمت دیگر پدیدار شود، تشخیص پارکینسون داده میشود مگر اینکه علایم دیگری همزمان وجود داشته باشد که بیماری دیگری را نمایان کند. بیمار ممکن است در اوایل، بیماری را با لرزش دست و پا یا با ضعیف شدن حرکت احساس کند و دریابد که انجام هر کاری بیشتر از حد معمول طول میکشد یا اینکه سختی و خشک شدن حرکت دست و ضعف تعادل را تجربه میکند. اولین نشانههای پارکینسون مجموعهای متفاوت از ارتعاش، برادیکنزیا، سفت شدن عضلات و تعادل ضعیف هستند. معمولاً علایم پارکینسون ابتدا در یک سمت بدن پدیدار میشوند و با گذشت زمان به سمت دیگر هم راه پیدا میکنند.
تغییراتی در حالت صورت و چهره روی میدهد، از جمله ثابت شدن (fixation) حالت صورت (ظاهراً احساسات کمی بر چهره نمایان میشود) یا حالت خیرگی چشم (به دلیل کاهش پلک زدن). علاوه بر اینها، خشک شدن شانه یا لنگیدن پا در سمت تحت تأثیر قرارگرفته عوارض دیگر (عادی) این بیماری است. افراد مسن ممکن است نمایان شدن یک به یک این نشانههای پارکینسون را به تغییرات افزایش سن ربط بدهند، ارتعاش را به عنوان «لرزش» بدانند، برادیکنزیا را به «آرام شدن عادی» و سفت شدن عضلات را به «آرتروز» ربط بدهند. حالت قوز (stooped) این بیماری را هم خیلی از این افراد به سن یا پوکی استخوان (osteoporosis) ربط میدهند. هم بیماران مسن و هم بیماران جوان ممکن است بعد از بیش از یک سال که با این عوارض روبرو بودهاند برای تشخیص به پزشک مراجعه کنند.
تشخیص
محققان آزمایشی ابداع کردهاند که در آن یک مولکول مرتبط با بیماری پارکینسون در نمونه مایع مغزی_نخاعیبیمار تشخیص داده میشود؛ این یافته میتواند راه را برای تشخیص زودهنگام این بیماری و تقویت چشمانداز درمان آن هموار کند. Bebnztropine دارویی که برای درمان تجویز میشود
درمان
این بیماری درمان قطعی ندارد اما داروهایی مثلاً لوودوپا(levodopa) آمانتادین، بیپریدن و سلژیلین در درمان آن تجویز میشود. گاه از جراحی نیز استفاده میشود. البته نقش کاردرمانی و فیزیوتراپی در این زمینه بسیار زیاد است زیرا مانع پیشرفت بیماری و محدودیت عملکرد میشود. تحقیقات جدید نشان داد خوردن مواد غذایی حاوی نیکوتین مانند فلفل و گوجه فرنگی به کاهش پارکینسون منجر میشود. محققان آمریکایی دریافتند: خوردن موادغذایی حاوی (حتی مقدار کم) نیکوتین، مانند فلفل و گوجه فرنگی، ممکن است خطر ابتلاء به بیماری پارکینسون را کاهش دهد. دکتر «سوزانسیرلس نیلسن» و همکارانش در دانشگاه واشینگتن در سیاتل ۴۹۰ نفر را که به تازگی به بیماری پارکینسون در درمانگاه دانشگاه مغز و اعصاب یا سازمان حفظ سلامت منطقهای تشخیص داده شده بودند را مورد بررسی قرار دادند.
از طرفی دیگر ۶۵۴ نفر از افراد بدون شرایط عصبی به عنوان گروه شاهد مورد استفاده قرار گرفت.
در این تحقیقات، شرکتکنندگان پرسشنامهای در رابطه با رژیم غذایی و استفاده از توتون و تنباکو را پر کردند.
محققان دریافتند که مصرف سبزیجات بهطور کلی خطر ابتلاء به بیماری پارکینسون تأثیر نمیگذارد، اما مصرف سولاناسه خوراکی-خانواده گیاه گلدار با برخی از گونههای تولید غذاهایی که منابع خوراکی از نیکوتین هستند- خطر ابتلاء به بیماری پارکینسون را کاهش دادهاست. این تحقیقات همچنین نشان داد که فلفل در کاهش بیماری پارکینسون قویتر عمل کردهاست. در این مورد سیگار و قلیان که منبع سرشار از نیکوتین هستند کمک قابل توجهی برای پیشگیری از این بیماری میکنند؛ ولی به دلیل خطر ابتلاء به بیماریهای خطرناک دیگر که توسط سیگار وقلیان در بدن ایجاد میشود، استفاده از این دخانیات توصیه نمیشود.
محققان در آزمایشی دیگر دریافتند گرمای مستعد شده از نمک دریایی به درمان این بیماری کمک میکند. دراین آزمایش مشخص شد ۷۰ نفر از شرکت کنندگان به طرز قابل توجهی بهبود یافتند. آنها از ترکیب نمک گرم شده با گرما بر روی سطح بدن خود استفاده کردند. استفاده از داغ درمانی بهطور قابل توجهی در حال افزایش است.
به تازگی محققان بیمارستان مک لین آمریکا با استفاده از داروهای درمان مالاریا، موفق به توقف بیماری پیشرونده پارکینسون شدند. این تحقیقات نشان میدهد که مغز دارای یک گیرنده پروتئینی به نام Nurr1 است که از سلولهایدوپامین محافظت میکند. دو مورد از داروهای درمان مالاریا که به تأیید سازمان غذا و داروی آمریکا (FDA) رسیدهاست، این گیرنده پروتئینی را مورد هدف قرار میدهد. در واقع جسم سیاه پیامهای عصبی را از طریق نخاع به عضلات مختلف ارسال میکند و این فرایند از طریق ماده شیمیایی دوپامین صورت میگیرد. استفاده از این داروها فرایند انتقال پیام عصبی به عضلات را تسهیل میکند

اختلال کمتوجّهی - بیشفعالی (به انگلیسی: Attention-deficit hyperactivity disorder)(به صورت مخفف: ADHD) یک اختلال رفتاری رشدی است.
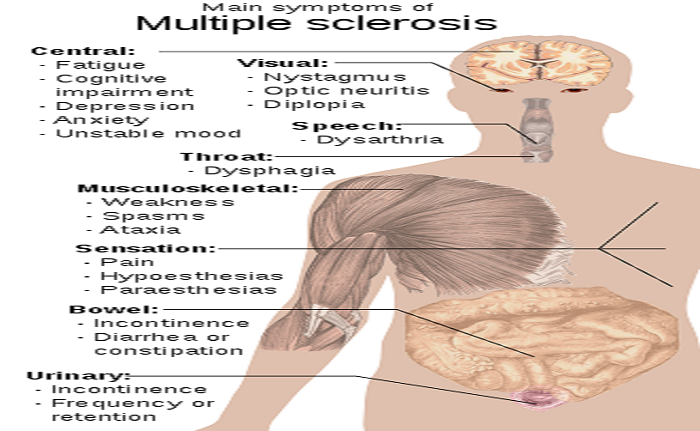
MS
اِماِس یا تصلب بافت چندگانه (به انگلیسی: Encephalomyelitis disseminata یا Multiple sclerosis) که با نام اختصاریِ اِماِس یا MS شناخته میشود،

اوتیسم یا درخودماندگی
نوعی اختلال رشدی (از نوع روابط اجتماعی) است که با رفتارهای ارتباطی و کلامی غیرطبیعی مشخص میشود.
سکته مغزی
نوعی اختلال نورولوژیک ناگهانی است که به علت عروق کانونی قابل انتساب است که به دنبال آن خونرسانی به ناحیهای که دچار سکته مغزی شدهاست مختل میشود.
فلج مغزی (به انگلیسی: cerebral palsy)
گروهی از اختلالات حرکتی دایم ولی غیر پیشرونده هستند که به دلیل ناهنجاریهای مادرزادی یا اسیبهای وارده بر مغز در مراحل اولیه تکامل ایجاد میگردند.
کادر درمانی مرکز توانبخشی نسیم به شرح زیر می باشد